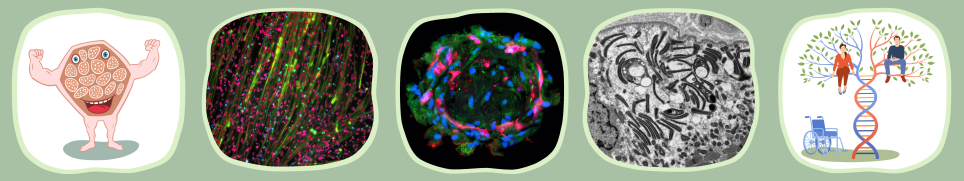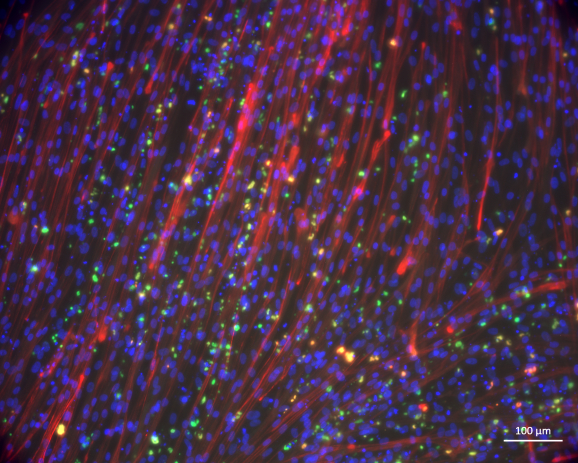
Myotubes dérivés de cellules souches pluripotentes induites humaines (hiPSC)
Myopathies génétiques et développement thérapeutique
Le Groupe 1, dirigé par E. MALFATTI, se concentre sur l’identification et la caractérisation approfondie de nouvelles myopathies génétiques et sur le développement de stratégies thérapeutiques pour ces maladies rares.
Un objectif majeur est la mise en place de registres de patients et d’études d’histoire naturelle, prérequis essentiels pour les futurs essais cliniques.
Parallèlement, le groupe poursuit la caractérisation clinique, histopathologique et génétique d’une large cohorte de patients suivis au Centre de Référence Neuromusculaire Henri Mondor de la Filière FILNEMUS (site web Henri Mondor – CRMRNM), dans le but d’identifier de nouveaux gènes pathogènes. Face à l’absence d’intérêt pharmaceutique pour les myopathies rares, le groupe développe activement des stratégies thérapeutiques innovantes, notamment une thérapie génique ciblant la myopathie liée à MYPN via vecteur AAV, testée in vitro sur des modèles de myofibres 3D et in vivo sur des souris knock-out pour myopalladine. Des stratégies de repositionnement de médicaments utilisant des modèles hiPSC dérivés de patients sont également mises au point pour identifier des cibles thérapeutiques exploitables pour des myopathies congénitales (CMYO) génétiques rares.
Ces approches intégrées visent à relier découverte génétique, modélisation des maladies et traduction thérapeutique pour les myopathies génétiques rares.
Reference:
1Malfatti E, Caramizaru A, Lee H, Kim J, Shoaito H, Pennisi A, Souvannanorath S, Authier FJ, Dumitrescu A, Fahmy N, Escobar-Cedillo RE, Miranda-Duarte A, Luna-Angulo AB, Nouioua S, Benchaabi O, Tazir M, Hallal S, Martinez P, Castiglioni C, Dobrescu A, Tajsharghi H. NEUROMYODredger: Whole Exome Sequencing for the Diagnosis of Neurodevelopmental and Neuromuscular Disorders in Seven Countries. Clin Genet. 2025 Feb 25;108(3):318-22. doi: 10.1111/cge.14736.
2Cardone N, Taglietti V, Baratto S, Kefi K, Periou B, Gitiaux C, Barnerias C, Lafuste P, Pharm FL, Pharm JN, Panicucci C, Desguerre I, Bruno C, Authier FJ, Fiorillo C, Relaix F, Malfatti E. Myopathologic trajectory in Duchenne muscular dystrophy (DMD) reveals lack of regeneration due to senescence in satellite cells. Acta Neuropathol Commun. 2023 Oct 19;11(1):167. doi: 10.1186/s40478-023-01657-z.
3 Onnée M, Malfatti E. The widening genetic and myopathologic spectrum of congenital myopathies (CMYOs): a narrative review. Neuromuscul Disord. 2025 Apr;49:105338. doi: 10.1016/j.nmd.2025.105338.
Maladies neuromusculaires acquises et myopathies immunitaires
Le Groupe 2, dirigé par F.J. AUTHIER, étudie la physiopathologie et le traitement des maladies neuromusculaires acquises à travers cinq axes principaux : myopathies immunitaires, interféronopathies, ciliopathies acquises, syndromes de fatigue chronique et atteintes musculaires liées au COVID-19.
Le muscle squelettique sain est continuellement soumis à des contraintes mécaniques, à des agents infectieux et à des xénobiotiques, susceptibles de déclencher inflammation, stress oxydatif ou dysfonctionnement métabolique. Des réponses inappropriées peuvent entraîner des altérations structurelles et fonctionnelles du muscle. Le groupe vise à décrypter les mécanismes moléculaires sous-jacents à ces troubles afin d’améliorer le diagnostic et de développer des approches thérapeutiques innovantes.
Un accent particulier est mis sur les maladies induites par les interférons, telles que la dermatomyosite juvénile et la myosite à inclusions (IBM). Dans l’IBM, l’infiltration persistante de lymphocytes T CD8 sécrétant l’IFNγ provoque une dégénérescence progressive du muscle et une résistance aux traitements immunosuppresseurs. Les travaux en cours incluent un essai clinique évaluant l’inhibiteur de JAK le ruxolitinib, et des études explorant le rôle du cil primaire. Des approches transcriptomiques avancées et des omiques spatiales sont utilisées pour revisiter la physiopathologie des myopathies inflammatoires et dysimmunes.
Grâce aux essais cliniques, aux analyses de données à grande échelle et aux études mécanistiques, cette recherche vise à identifier de nouvelles cibles thérapeutiques et à améliorer le pronostic des patients atteints de maladies neuromusculaires acquises, notamment à travers l’essai clinique BIGTIM, un essai de phase IIb évaluant le blocage de l’interféron-γ par le ruxolitinib dans la myosite à inclusion, dont l’objectif principal est d’améliorer les performances locomotrices globales après un an de traitement, mesurées par une augmentation supérieure à 60 m au test de marche de 6 minutes (6MWT).
Reference:
1Martin L, Kaci N, Benoist-Lasselin C, Mondoloni M, Decaudaveine S, Estibals V, Cornille M, Loisay L, Flipo J, Demuynck B, de la Luz Cádiz-Gurrea M, Barbault F, Fernández-Arroyo S, Schibler L, Segura-Carretero A, Dambroise E, Legeai-Mallet L.
Theobroma cacao improves bone growth by modulating defective ciliogenesis in a mouse model of achondroplasia. Bone Research. 2022;10(1):8. doi:10.1038/s41413-021-00177-7. PMID:35078974
2Martin L*, Cogné B*, Latypova X*, Senaratne LDS*, Koboldt DC, Kellaris G, Fievet L, Le Meur G, Caldari D, Debray D, Nizon M, Frengen E, Bowne SJ; 99 Lives Consortium; Cadena EL, Daiger SP, Bujakowska KM, Pierce EA, Gorin M, Katsanis N, Bézieau S, Petersen-Jones SM, Occelli LM, Lyons LA, Legeai-Mallet L, Sullivan LS, Davis EE, Isidor B.
Mutations in the Kinesin-2 Motor KIF3B Cause an Autosomal-Dominant Ciliopathy. American Journal of Human Genetics. 2020;106(6):893–904. doi:10.1016/j.ajhg.2020.04.005. PMID:32386558
3Tragin M, Degrelle SA, Periou B, Bader-Meunier B, Barnerias C, Bodemer C, Desguerre I, Rodero MP, Authier FJ, Gitiaux C.
Muscle Spatial Transcriptomic Reveals Heterogeneous Profiles in Juvenile Dermatomyositis and Persistence of Abnormal Signature After Remission. Cells. 2025;14(12):939. doi:10.3390/cells14120939. PMID:40558566; PMCID: PMC12190613
4Hou C, Periou B, Gervais M, Martin L, Berthier J, Baba-Amer Y, Souvannanorath S, Lechapt-Zalcman E, Malfatti E, Gherardi RK, Relaix F, Bencze M, Authier FJ.
Interferon-γ causes myogenic cell dysfunction and senescence in immune myopathies. Brain. 2025;148(8):2883–2898. doi:10.1093/brain/awaf153. PMID:40296760
Stratégies thérapeutiques et de bio-ingénierie basées sur les cellules souches musculaires pour les troubles neuromusculaires
Le Groupe 3, dirigé par N. DIDIER, explore le potentiel des cellules souches musculaires comme cibles thérapeutiques pour les maladies neuromusculaires, ainsi que leurs applications en thérapie cellulaire et en ingénierie tissulaire.
Un axe majeur du groupe est l’étude du rôle des cellules souches musculaires dans l’amyotrophie spinale (SMA). En combinant des approches d’ingénierie tissulaire, multi-omiques, et des modèles animaux, le groupe s’intéresse en particulier aux interactions entre les cellules souches musculaires, les jonctions neuromusculaires et les motoneurones, afin de développer des stratégies thérapeutiques combinatoires pour maintenir la fonction neuromusculaire sur le long terme.
D’autres axes de recherche du groupe visent à : 1) Développer des stratégies pharmacologiques pour préserver le potentiel thérapeutique des cellules souches musculaires humaines durant leur expansion in vitro; 2) Développer des modèles de muscles en 3D pour étudier les mécanismes moléculaires précoces des maladies neuromusculaires et tester de nouvelles thérapies; 3) Élaborer des stratégies de médecine régénérative pour réparer les lésions musculaires à partir de matrices biomimétiques combinées à des cellules myogéniques dérivées de cellules souches musculaires humaines ou de cellules souches pluripotentes induites.
Ces approches placent les cellules souches musculaires au cœur de thérapies régénératives et translationnelles innovantes pour les troubles neuromusculaires
Reference:
1Ozturk T, Mignot J, Gattazzo F, Gervais M, Relaix F, Rouard H, Didier N.
Dual inhibition of P38 MAPK and JNK pathways preserves stemness markers and alleviates premature activation of muscle stem cells during isolation. Stem Cell Research & Therapy. 2024;15(1):179.
2Mecca J, Mignot J, Gervais M, Ozturk T, Astord S, Berthier J, Bauché S, Messéant J, Biferi MG, Rouard H, Barkats M, Relaix F, Didier N.
Targeted knockdown of SMN in muscle stem cells induces non-cell autonomous loss of motor neurons. bioRxiv (2024). doi:10.1101/2024.12.19.629483. Accepted in Brain (January 2026).
Ingénierie tissulaire du tendon et de l’os
Le Groupe 4, dirigé par H. ROUARD, se concentre sur l’ingénierie tissulaire du tendon et de l’os.
Les tendons assurent la jonction mécanique entre le muscle et l’os, mais leur réparation spontanée est limitée par une vascularisation insuffisante. Les réparations chirurgicales des ruptures tendineuses sont souvent associées à des complications, telles que la restriction de mouvement, la formation de tissu cicatriciel, la douleur chronique et les ruptures secondaires. Le groupe développe des substituts tendineux issus de l’ingénierie tissulaire pour favoriser une guérison robuste de la jonction ostéotendineuse et limiter les complications post-opératoires.
Ces travaux utilisent des cellules stromales dérivées de tissu adipeux (ADSC), facilement accessibles et capables de se différencier en tendinocytes. L’objectif est de générer un tendon artificiel biohybride composé d’ADSC pré-différenciées vers un phénotype tendineux et cultivées dans des échafaudages tridimensionnels. Ces constructions seront évalués dans des modèles précliniques de rupture du tendon d’Achille. Une attention particulière est portée à l’amélioration de l’ancrage tendon-os grâce à l’utilisation d’interfaces en titane poreux, développées en collaboration avec le Groupe 5 (N. Chevallier).
Ces études précliniques sont réalisées en étroite collaboration avec des chirurgiens orthopédistes et bénéficient de plateformes de production tissulaire conformes aux normes GMP, avec l’objectif à long terme de développer un médicament de thérapie innovante.
Ingénierie osseuse et stratégies régénératives
Le Groupe 5, dirigé par N. CHEVALLIER.
Notre groupe développe des approches innovantes pour améliorer la prise en charge des défauts osseux importants ou complexes, qui représentent encore un défi clinique majeur. Les cellules stromales mésenchymateuses (CSM) constituent le cœur de nos stratégies, et leur potentiel a été démontré dans plusieurs essais cliniques (FP7 REBORNE, H2020 Maxibone). Malgré ces avancées, la consolidation osseuse reste souvent lente ou incomplète, en particulier dans les reconstructions de grande taille ou de géométrie complexe.
Nos recherches s’organisent autour de quatre axes principaux :
- Analyse des mécanismes de la régénération osseuse induite par les CSM, à l’aide de modèles animaux et d’approches multi‑omiques. Ces travaux visent à identifier les voies cellulaires et moléculaires impliquées dans la chimiotaxie, la différenciation ostéogénique, l’angiogenèse et la mise en place d’un microenvironnement propice à la réparation tissulaire.
- Développement de substituts osseux prévascularisés issus d’une source cellulaire unique. Nous combinons organoïdes osseux-vascularisés, biomatériaux bioactifs et biomatériaux issus de l’impression 3D pour générer des constructions permettant une anastomose vasculaire rapide, une meilleure survie cellulaire post‑implantation et une ossification homogène. Ces modèles serviront également de plateformes in vitro pour l’étude des interactions cellules‑cellules dans des modèles sains ou pathologiques ainsi que pour des études de réponses aux molécules thérapeutiques.
- Élaboration de protocoles universels basés sur les cellules iPS, afin de produire des lignées endothéliales et ostéo‑compétentes standardisées, sécurisées et compatibles avec une utilisation clinique. Ces travaux incluent l’optimisation des étapes de différenciation, de maturation tissulaire et de contrôle qualité.
- Faciliter l’utilisation clinique des médicaments de thérapie innovante (MTI) en optimisant les procédés de production, de conservation et de logistique.
Ensemble, ces approches visent à accélérer la régénération osseuse, à améliorer la faisabilité des reconstructions complexes et à rendre les thérapies cellulaires et tissulaires plus accessibles en clinique.
Reference:
¹ Marie T, Cojocaru AI, Coquelin L, Varaillon E, Rouard H, Chevallier N. Directly thawed bone marrow mesenchymal stromal cells retain mechanism of action and support bone clinical translation. Stem Cell Reviews and Reports. 2025; Epub ahead of print. doi:10.1007/s12015-025-11025-0. PMID: 41398484.
² Sanz M, Gjerde C, Gjertsen BT, Ortiz-Vigón A, Sanchez N, Hoornaert A, et al. Bone augmentation of atrophic alveolar ridges using a synthetic bone substitute with mesenchymal stem cells: a randomized, controlled clinical trial. Clinical Oral Implants Research. 2025; Epub ahead of print. doi:10.1111/clr.70025. PMID: 40844304.
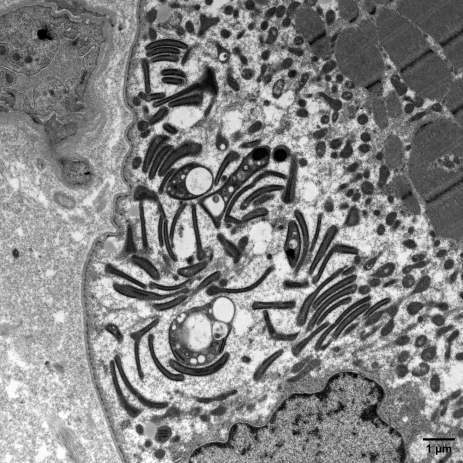
Micrographie électronique montrant des mitochondries anormales