Projet de recherche
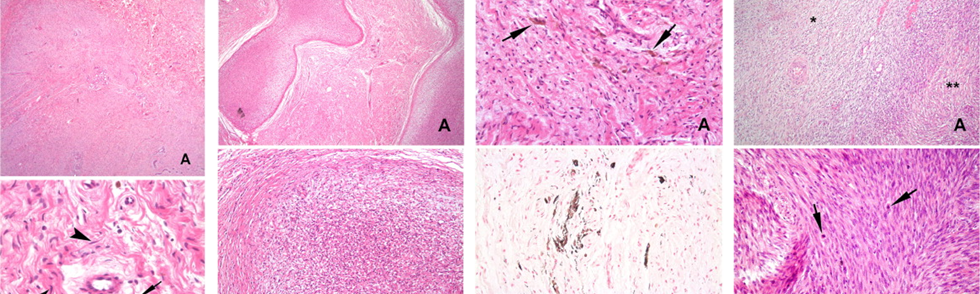
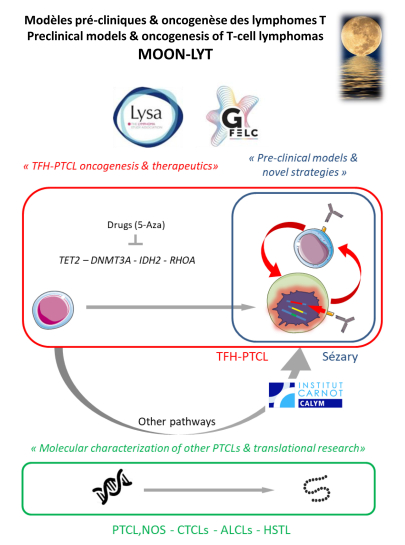 Le projet scientifique de l’équipe est axé sur la caractérisation des mécanismes moléculaires et cellulaires régissant le développement des lymphomes, en particulier les lymphomes T périphériques, incluant les lymphomes T cutanés. Les deux modèles d’étude principaux sont les lymphomes dérivés des cellules T helper folliculaires ou lymphomes TFH (dont le chef de file est le lymphome T angio-immunoblastique), lymphome le plus fréquent en occident, et le syndrome de Sézary, permettant un accès facilité à des cellules tumorales viable grâce à son expression leucémique. L’équipe est riche d’investigateurs principaux reconnus internationalement dans les domaines de l’oncogenèse des lymphomes T périphérique et cutanés (Professeurs Philippe Gaulard, François Lemonnier, Marie-Hélène Delfau, Corinne Haioun, David Sibon et Nicolas Ortonne) et globalement d’une équipe multidisciplinaire aux compétences très complémentaires.
Le projet scientifique de l’équipe est axé sur la caractérisation des mécanismes moléculaires et cellulaires régissant le développement des lymphomes, en particulier les lymphomes T périphériques, incluant les lymphomes T cutanés. Les deux modèles d’étude principaux sont les lymphomes dérivés des cellules T helper folliculaires ou lymphomes TFH (dont le chef de file est le lymphome T angio-immunoblastique), lymphome le plus fréquent en occident, et le syndrome de Sézary, permettant un accès facilité à des cellules tumorales viable grâce à son expression leucémique. L’équipe est riche d’investigateurs principaux reconnus internationalement dans les domaines de l’oncogenèse des lymphomes T périphérique et cutanés (Professeurs Philippe Gaulard, François Lemonnier, Marie-Hélène Delfau, Corinne Haioun, David Sibon et Nicolas Ortonne) et globalement d’une équipe multidisciplinaire aux compétences très complémentaires.
L’équipe s’intéresse à la nature et aux conséquences fonctionnelles des altérations moléculaires caractérisant les cellules tumorales en portant une attention particulière à la hiérarchie des événements génétiques, à la nature des cellules impliquées dans les événements initiateurs, leurs aberrations phénotypiques/moléculaires et les interactions des cellules tumorales avec leur environnement. Les analyses moléculaires que nous menons actuellement bénéficient de technologies de pointe, comme le séquençage de cellule unique (« single cell ») ou l’étude de tumeurs par techniques spatiales multiplexées. Nous développons également des preuves de concept in vitro et ex vivo pour de nouvelles approches thérapeutiques, en tirant profit de modèles d’étude pré-cliniques établis à partir de lignées, de cellules primaires et de modèles murins.
Ces projets ont pour objectif final l’identification de nouvelles cibles ou concepts thérapeutiques à base d’inhibiteurs chimiques ou d’anticorps monoclonaux, qui permettront d’améliorer la prise en charge des patients atteints de lymphomes T.
Au delà de notre intégration dans l’institut Mondor, avec accès à ses différentes plateformes techniques, les travaux que nous menons s’appuient tout particulièrement sur :
– Les cohortes de patients annotés issus des essais cliniques du LYSA (LYmphoma Study Association) dont des membres de l’équipe sont membres du bureau (F Lemonnier, C Haioun et MH Delfau) ;
– Les collections d’échantillons de tumeurs disponibles sur le site Henri Mondor, conservées dans la plateforme de ressource biologique, en lien avec des réseaux d’expertise nationaux labellisés par l’INCa (Lymphopath et Réseau national des Lymphomes Cutanés [RNLC] du Groupe Français d’Etude des Lymphomes Cutanés [GFELC], en partie coordonné par le Pr N. Ortonne), établies à partir de projets de recherche nationaux (PHRC TENOMIC, Pr P. Gaulard et KIRs, Pr N Ortonne),…), ou prospectives (collection de lymphomes cutanés, LYCUT) ;
– Des interactions avec des partenaires académiques (International Lymphoma Study Group dont N Ortonne est membre élu), des sociétés savantes (EHA, EORTC-CLTG,…) et agences de financement de la recherche à l’échelle nationale et internationale ;
– Des partenariats/collaborations industriels, en partie par l’intermédiaire de l’Institut Carnot CALYM;

– L’établissement de modèles murins développés par l’équipe (souris xénogreffées de type PDX ou CDX) ;
– Des brevets portant sur de nouvelles cibles ou nouveaux concepts thérapeutiques pour les lymphomes T.