Groupe Génomique
 Axes de recherche
Axes de recherche
Il est largement démontré que les facteurs génétiques contribuent fortement au risque de développer la plupart des troubles psychiatriques. Notre groupe travaille depuis de nombreuses années à la caractérisation de l’architecture génétique des troubles bipolaires, de la schizophrénie ou des troubles dépressifs majeurs ainsi qu’à l’identification de marqueurs génétiques et biologiques qui permettraient de prédire l’évolution de la maladie ou de sélectionner le traitement le plus adapté à la physiologie des personnes malades.
Notre exploration est basée principalement sur des approches de génotypage à haut-débit, de séquençage d’exomes ou de génomes, d’analyses de transcriptome et de méthylome.
Nous avons développé ces dernières années trois axes de recherche autour de (i) l’architecture génétique des troubles psychiatriques pour estimer le risque individuel de développer un trouble ou de répondre à un traitement, (ii) des liens entre les facteurs génétiques et les mécanismes moléculaires qui sont à l’origine de ces troubles notamment par développement de modèles animaux et d’organoïdes cérébraux et (ii) par l’exploration de facteurs environnementaux dans la vulnérabilité aux troubles psychiatriques avec une recherche autour des effets de la pollution atmosphérique sur le développement cérébral et le risque de développer un trouble psychiatrique.
 Résultats récents
Résultats récents
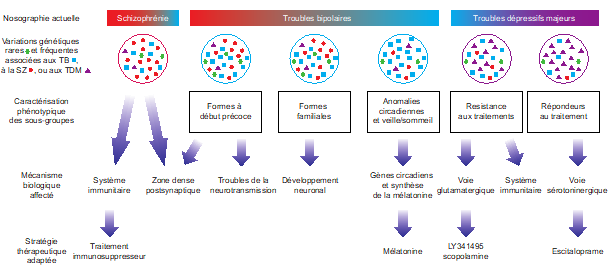
Notre contribution avec de nombreux autres groupes de recherche au Psychiatric Genomics Consortium a permis ces dernières années l’identification de nombreux loci associés au risque de développer un trouble bipolaire (Jamain et al., 2014 ; Mullins et al., 2021), mais également de montrer les liens génétiques qui existent entre les troubles bipolaires, la schizophrénie et les troubles dépressifs majeurs (Cross-Disorder Group of the Psychiatric Genomics Consortium, 2019 ; Courtois et al., 2020). Nous avons pu ainsi caractériser des sous-groupes homogènes sur le plan clinique qui présentent des disfonctionnements des mêmes mécanismes moléculaires.
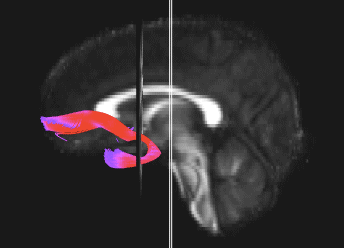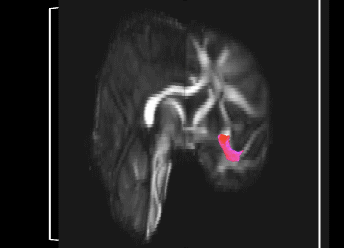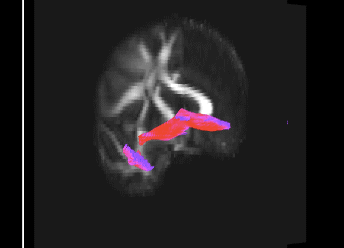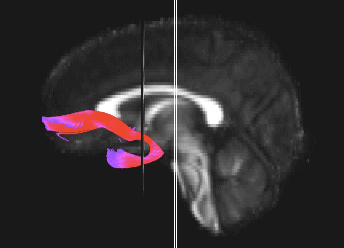
Faisceau montrant la connectivité fonctionnelle entre le cortex préfrontal ventro-médian et l’amygdale. Le génotype à risque du rs6039769 situé dans le promoteur de SNAP25 est associé à une augmentation de cette connectivité chez les hommes.
L’exploration fonctionnelle des variations génétiques rares et fréquentes associées aux troubles bipolaires nous ont révélé l’importance des mécanismes de neurotransmission chez les personnes avec des formes à début précoce de trouble bipolaire (Etain et al., 2010 ; Houenou et al., 2017). En particulier, nous avons montré que ces mécanismes étaient associés à des modifications de la structure de l’amygdale et de la connectivité entre celle-ci et le cortex préfrontal ventro-médian chez les personnes porteuses de génotype à risque de développer un trouble bipolaire dans le gène SNAP25 (Houenou et al. 2017). Nous avons également montré que des variations génétiques altérant la fonction de CADPS, une protéine sensible au calcium et nécessaire pour la libération de neurotransmetteurs, étaient associées à une plus grande sensibilité au stress aussi bien chez l’homme que chez la souris (Sitbon et al. in press).
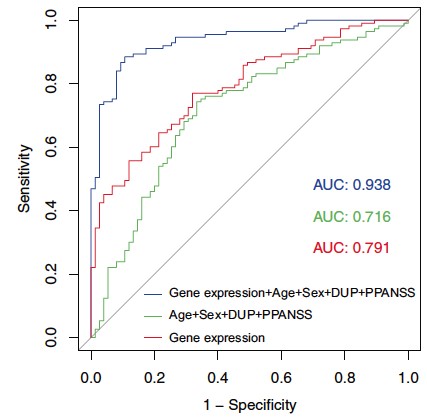 Au travers de la caractérisation génétique de sous-groupes homogènes de personnes avec des troubles psychiatriques partageant des facteurs de vulnérabilité, notre objectif est de proposer des stratégies thérapeutiques adaptées aux mécanismes moléculaires perturbés chez les personnes malades. En ce sens, nous avons montré que l’expression de certains gènes au niveau du sang périphérique permettait de prédire la réponse à un traitement antipsychotique lors d’un premier épisode de psychose et que cette prédiction était encore plus fiable lorsqu’elle était combinée aux données cliniques et environnementales collectées chez les personnes malades (Troudet et al., 2020).
Au travers de la caractérisation génétique de sous-groupes homogènes de personnes avec des troubles psychiatriques partageant des facteurs de vulnérabilité, notre objectif est de proposer des stratégies thérapeutiques adaptées aux mécanismes moléculaires perturbés chez les personnes malades. En ce sens, nous avons montré que l’expression de certains gènes au niveau du sang périphérique permettait de prédire la réponse à un traitement antipsychotique lors d’un premier épisode de psychose et que cette prédiction était encore plus fiable lorsqu’elle était combinée aux données cliniques et environnementales collectées chez les personnes malades (Troudet et al., 2020).
Publications récentes
Mullins N, Forstner AJ, O'Connell KS, Coombes B, Coleman JRI, et al. Genome-wide association study of more than 40,000 bipolar disorder cases provides new insights into the underlying biology.
Nat Genet. 2021 Jun;53(6):817-829. doi: 10.1038/s41588-021-00857-4.Schürhoff F, Corfdir C, Pignon B, Lajnef M, Richard JR, Marcos E, Pelissolo A, Leboyer M, Adnot S, Jamain S, Szöke A. No alteration of leukocyte telomere length in first episode psychosis.
Psychiatry Res. 2021 Jul;301:113941. doi: 10.1016/j.psychres.2021.113941.Pollak TA, Vincent A, Iyegbe C, Coutinho E, Jacobson L, Rujescu D, Stone J, Jezequel J, Rogemond V, Jamain S, Groc L, David A, Egerton A, Kahn RS, Honnorat J, Dazzan P, Leboyer M, McGuire P. Relationship Between Serum NMDA Receptor Antibodies and Response to Antipsychotic Treatment in First-Episode Psychosis.
Biol Psychiatry. 2021 Jul 1;90(1):9-15. doi: 10.1016/j.biopsych.2020.11.014.El Yacoubi M, Vaugeois JM, Jamain S. Antidepressant-like effect of low dose of scopolamine in the H/Rouen genetic mouse model of depression.
Fundam Clin Pharmacol. 2021 Aug;35(4):645-649. doi: 10.1111/fcp.12639.Szoke A, Pignon B, Boster S, Jamain S, Schürhoff F. Schizophrenia: Developmental Variability Interacts with Risk Factors to Cause the Disorder: Nonspecific Variability-Enhancing Factors Combine with Specific Risk Factors to Cause Schizophrenia.
Bioessays. 2020 Nov;42(11):e2000038. doi: 10.1002/bies.202000038.Troudet R, Ali WBH, Bacq-Daian D, Rossum IWV, Boland-Auge A, Battail C, Barau C; OPTiMiSE study group, Rujescu D, McGuire P, Kahn RS, Deleuze JF, Leboyer M, Jamain S. Gene expression and response prediction to amisulpride in the OPTiMiSE first episode psychoses.
Neuropsychopharmacology. 2020 Sep;45(10):1637-1644. doi: 10.1038/s41386-020-0703-2.Courtois E, Schmid M, Wajsbrot O, Barau C, Le Corvoisier P, Aouizerate B, Bellivier F, Belzeaux R, Dubertret C, Kahn JP, Leboyer M, Olie E, Passerieux C, Polosan M, Etain B, Jamain S; and the FondaMental Advanced Centers of Expertise in Bipolar Disorders (FACE-BD). Contribution of common and rare damaging variants in familial forms of bipolar disorder and phenotypic outcome.
Transl Psychiatry. 2020 Apr 28;10(1):124. doi: 10.1038/s41398-020-0783-0.Cross-Disorder Group of the Psychiatric Genomics Consortium. Genomic Relationships, Novel Loci, and Pleiotropic Mechanisms across Eight Psychiatric Disorders.
Cell. 2019 Dec 12;179(7):1469-1482.e11. doi: 10.1016/j.cell.2019.11.020.Houenou J, Boisgontier J, Henrion A, d'Albis MA, Dumaine A, Linke J, Wessa M, Daban C, Hamdani N, Delavest M, Llorca PM, Lançon C, Schürhoff F, Szöke A, Le Corvoisier P, Barau C, Poupon C, Etain B, Leboyer M, Jamain S. A Multilevel Functional Study of a SNAP25 At-Risk Variant for Bipolar Disorder and Schizophrenia.
J Neurosci. 2017 Oct 25;37(43):10389-10397. doi: 10.1523/JNEUROSCI.1040-17.2017.Jamain S, Cichon S, Etain B, Mühleisen TW, Georgi A, Zidane N, Chevallier L, Deshommes J, Nicolas A, Henrion A, Degenhardt F, Mattheisen M, Priebe L, Mathieu F, Kahn JP, Henry C, Boland A, Zelenika D, Gut I, Heath S, Lathrop M, Maier W, Albus M, Rietschel M, Schulze TG, McMahon FJ, Kelsoe JR, Hamshere M, Craddock N, Nöthen MM, Bellivier F, Leboyer M. Common and rare variant analysis in early- onset bipolar disorder vulnerability.
PLoS One. 2014 Aug 11;9(8):e104326. doi: 10.1371/journal.pone.0104326.