Dernières actualités de l’équipe
Dernières actualités de l’équipe
 12 novembre 2025:
12 novembre 2025:
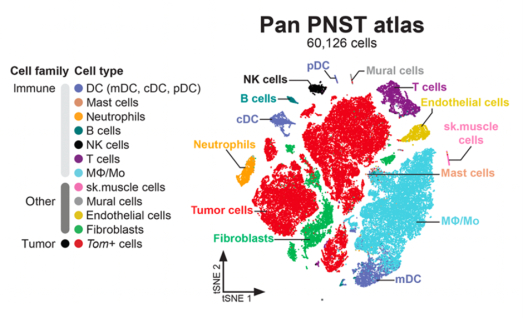
L’article “Glial-to-mesenchymal transition of tumor Schwann cells drives the genetic burden in MPNSTs from neurofibromatosis type 1 mouse model” par Radomska KJ, Onfroy A, Lecerf L, Job B, Beaude A, Sesma Sanz L, El Jalkh T, Thieffry D, Charnay P, Wolkenstein P, Ortonne N, Coulpier F, et Topilko P. a été publié dans le journal Science Advances, 2025 Nov 12, Vol 11, Issue 45, DOI: 10.1126/sciadv.adt9210
Cet article reconstitue l’évolution des tumeurs malignes des gaines nerveuses périphériques, identifie la transition gliale maligne comme un facteur clé et met en évidence Sox9 comme cible thérapeutique.
 16 décembre 2025:
16 décembre 2025:
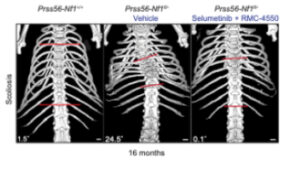
L’article “Pharmacological inhibition of RAS pathway alleviates spine deformity in a mouse model of neurofibromatosis type 1” par Kovaci F, Goachet C, Perrin S, Slimani L, Coulpier F, Tilotta F, Topilko P et Colnot C a été published dans le journal Bone Research, 2025 Dec 16;13(1):103, DOI: 10.1038/s41413-025-00492-3
Dans cet article, nous avons analysé les déformations de la colonne vertébrale dans le modèle murin Prss56-Nf1 KO, modélisant la pathologie neurofibromatose de type 1 (NF1). Il s’agit du premier modèle reproduisant les anomalies de la colonne vertébrale associées à d’autres symptômes de cette pathologie, ce qui permet d’utiliser ce modèle pour des études précliniques. Nous avons montré que les inhibiteurs de la voie de signalisation RAS-MAPK peuvent en effet prévenir les déformations de la colonne chez les souris, ce qui suggère des stratégies thérapeutiques pour ces symptômes.
 29 janvier 2026:
29 janvier 2026:
Félicitations à Maria Ethel et à Cassandre Goachet pour leurs prix de posters à la Gordon Research Conference Bones and Teeth, à Galveston, TX. https://www.grc.org/bones-and-teeth-conference/2026/
Maria Ethel a présenté son projet sur un “atlas des cellules stromales musculosquelettiques”, et Cassandre Goachet a présenté ses “analyses épigénétiques des cellules souches/progénitrices squelettiques”.